La peste porcine classique (PPC) est une maladie infectieuse et contagieuse des suidés, due à un virus de la famille des Flaviviridae (genre Pestivirus).
ESPÈCES AFFECTES
- Suidés domestiques et sauvages (sangliers);
- Non transmissible à l’Homme.
ÉTIOLOGIE
- Proche des virus de la maladie des muqueuses et de la maladie de la frontière (border disease)
- Absence d’analogie avec le virus (virus à ADN) de la PPA;
- Plusieurs génogroupes : intérêt épidémiologique pour déterminer l’origine d’un foyer;
- Induit in vivo la formation d’anticorps neutralisants protecteurs.
ÉTUDE CLINIQUE
Incubation : 4 à 27 jours, parfois plus longue dans certaines formes atypiques.
Symptômes :
Forme typique
Maladie cliniquement indifférenciable de la PPA:
- Forme suraiguë : apparition brutale sans prodrome d’une fièvre importante associée à un état typhique, et mort en 24-48 h (sans symptôme cutané : « peste blanche »).
- Forme aiguë : fièvre (avec hyperthermie de l’ordre de 41°C) et prostration , symptômes locaux isolés ou diversement associés : blépharo-conjonctivite, symptômes cutanés (cyanose, congestion ou purpura dans les zones à peau fine), gastro-entérite, symptômes respiratoires (congestion pulmonaire) et/ou symptômes nerveux (ataxie, paralysie…). La mort survient généralement en 6 à 20 jours.
- Formes subaiguës ou chroniques : 3 périodes :
- dure 10 à 15 jours, marquée par une atteinte générale et des symptômes locaux (idem forme aiguë) atténués.
- phase de rémission.
- due à des bactéries de surinfection, associe une nouvelle atteinte de l’état général et des troubles locaux respiratoires, digestifs ou mixtes (pneumo-entérite, souvent d’origine salmonellique). Les animaux maigrissent et meurent en 1 à 3 mois.
Formes atypiques
Elles s’expriment sous des aspects très variés, par exemple :
Troubles de la reproduction et pathologie néonatale (avortements, mise bas de porcelets mort-nés ou momifiés, malformations responsables de tremblement congénital, splay leg, mortalité néonatale.
NB. Mise bas possible de porcelets immunotolérants atteints d’infection persistante, les premiers symptômes, puis la mort, survenant vers l’âge de 3 à 4 semaines (parfois 20 à 28 semaines).
- Formes frustes sur porcs à l’engrais ou futurs reproducteurs : retards de croissance, poussées thermiques, quelques cas de mortalité,…
- Formes inapparentes : circulation éventuelle de virus dans l’élevage (porcs à l’engrais) avec parfois éclosion de cas cliniques après l’intervention de causes favorisantes. Fréquentes chez le sanglier adulte (la PPC y est rarement exprimée cliniquement, sauf si la souche est très virulente).
LÉSIONS
Non constantes (les lésions hémorragiques les plus caractéristiques peuvent être absentes) et non spécifiques.
Formes de peste « typique » :
- Lésions congestives ou hémorragiques :
Les plus caractéristiques siègent sur les nœuds lymphatiques, les reins, la rate, la vessie et les amygdales.
- Les nœuds lymphatiques dans 85% des cas, précoce, (isolée ou généralisée). hypertrophiés et présentent des « marbrures » (congestives ou hémorragiques – aspect d’une « fraise coupée » à la coupe). Parfois totalement hémorragiques ( caillot sanguin ou une « cerise mûre »).
- Les reins ne sont pas hypertrophiés, piqueté hémorragique pétéchies ou de suffusions en quantité sur reins décolorés (après décapsulation). De nombreuses suffusions peuvent conférer aux reins un aspect en « œuf de dinde ».
- La rate, rarement hypertrophiée, zones d’infarcissement (parfois des hématomes) situées à sa périphérie et en déformant le bord.
- La vessie piquetée hémorragique (pétéchies, suffusions visibles après évagination pour en examiner la muqueuse), voire une infiltration hémorragique.
- Les amygdales : hypertrophiées, hémorragiques et parfois phénomènes ulcératifs. piqueté hémorragique peut être observé sur la muqueuse laryngée et l’épiglotte.
- L’atteinte congestive et hémorragique d’autres organes (peau, poumons, tube digestif) est fréquente, mais moins significative de peste que dans les cas précédents.
- Lésions ulcéreuses : sur la muqueuse du tube digestif (valvule iléo-caecale), le colon et le caecum (ulcères plats, arrondis, non perforants, recouverts d’un enduit fibrino-nécrotique), un stade tardif de l’évolution de la maladie dans les formes aiguës et surtout dans les formes sub-aiguës et chroniques. Elles résultent d’une nécrose succédant aux lésions hémorragiques, en particulier dans les formations lymphoïdes.
- Lésions de complications : lésions secondaires d’origine bactérienne (pneumonie, pneumo-entérite, entérite, gastrite croupale).
Formes de peste « atypique » :
lésions variées et non spécifiques (hémorragies cutanées, adénites avec parfois piqueté hémorragique, lésions de tératogenèse (hypoplasie cérébelleuse…).
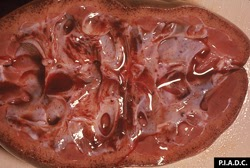
rein. Le cortex contient des pétéchies disséminées. Les calyces sont modérément dilatés (hydronéphrose) et contiennent également des hémorragies
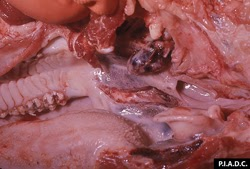
ganglion rétropharyngé. Le ganglion lymphatique est nettement élargi et hémorragique; l’amygdale contient plusieurs hémorragies mal démarquées
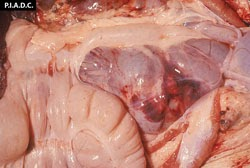
rein. Il y a une hémorragie étendue sur la surface corticale
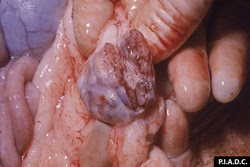
ganglion inguinal. Il existe des hémorragies pétéchiales et périphériques (sinus médullaire)
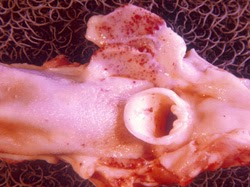
pharynx et larynx. Des hémorragies pétéchiales et des nécroses se développent dans les amygdales palatines et les muqueuses pharyngée et laryngée adjacentes
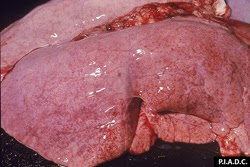
poumons. Les pétéchies pleurales disséminées sont nombreuses et il existe un léger œdème interlobulaire.
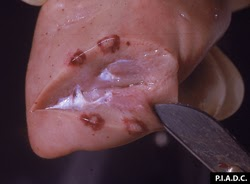
rein. Le cortex contient de multiples pétéchies et infarctus pâles entourés d’hémorragies
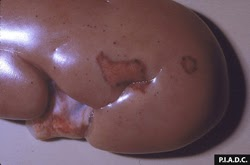
rein. Le cortex contient de multiples pétéchies et infarctus pâles entourés d’hémorragies.
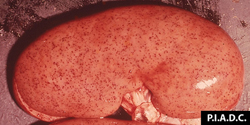
rein. Il existe de nombreuses pétéchies corticales disséminées (« rein d’œuf de dinde »)
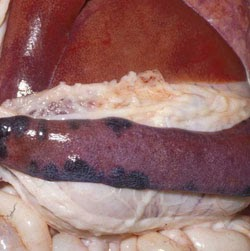
rate. Il existe de multiples infarctus coalescents, gonflés et rouge foncé le long des marges
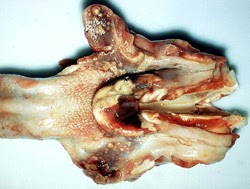
amygdales. L’épiglotte et l’amygdale palatine bissectée contiennent de multiples foyers de nécrose bronzés
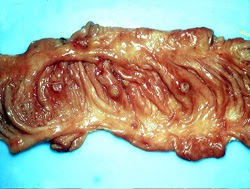
amygdales. L’épiglotte et l’amygdale palatine bissectée contiennent de multiples foyers de nécrose bronzés
ÉPIDÉMIOLOGIE
Sources de virus
- suidés (porcs ou sangliers) infectés malades, porteurs précoces (excrétion dès la phase de virémie, parfois 24 heures après leur contamination), porteurs chroniques (portage plusieurs semaines parfois après guérison) ou sains (infection inapparente de porcs à l’engrais, porcelets avec infection persistante…).
- tous les tissus, sécrétions et excrétions sont virulents (y compris le sperme).
- viandes et produits de charcuterie issus de porcs infectés (facteurs de diffusion de la maladie à grande distance).
Virus très résistant
- dans l’environnement (2 à 3 semaines)
- dans les locaux d’élevage (1 ou 2 mois)
- dans le purin ou le lisier et dans les viandes (jusqu’à 85 jours dans la viande réfrigérée et 4 ans dans la viande congelée)
- ou produits de charcuterie ( jusqu’à 188 jours dans la viande salée ou fumée…).
Transmission :
Les voies de pénétration du virus sont surtout buccale, nasale et transplacentaire (infection congénitale).
- Directe (contact)
- indirecte (environnement souillé, eaux grasses ou déchets d’origine porcine, divers intermédiaires souillés tels que les vêtements, véhicules…).
- transmission verticale congénitale : parfois incriminée dans la persistance des souches hypovirulentes.
- diffusion possible par la semence de verrats infectés.
Facteurs de sensibilité :
- sensibilité importante des jeunes favorisée (stress d’élevage) ;
- l’immunité colostrale peut retarder l’expression clinique des porcelets contaminés in utero.
Remarque : Chez le sanglier sauvage, les jeunes animaux la sous population la plus sensible et la plus affectée par la maladie (létalité atteignant 70 à 90 % chez les marcassins infectés dans les Vosges) et potentiellement la plus excrétrice de virus. L’entretien et la propagation de l’épizootie sont favorisés par une forte densité de sangliers. La propagation peut être en outre facilitée par des actions de chasse favorisant le déplacement et la dispersion des compagnies.
DIAGNOSTICS DIFFÉRENTIELS
- le diagnostic clinique différentiel PPC/PPA n’étant pas possible. Ils conduisent à une suspicion de « peste porcine ».
- relations épidémiologiques avec un pays infecté, phénomènes hémorragiques intenses, œdème de la paroi de la vésicule biliaire, etc.
Attention : Le diagnostic différentiel des pestes porcines classique ou africaine ne peut se faire que sur diagnostic de laboratoire.
Le diagnostic différentiel avec d’autres maladies dites « rouges » est très délicat sur le terrain sans avoir recours à un diagnostic de laboratoire, seul un contexte épidémiologique particulier pourrait orienter la suspicion vers une autre maladie comme le SDRP, la dermatite néphrite (PDNS) due au circovirus porcin de type 2 ou d’autres maladies bactériennes comme celles dues à Streptococcus suis, Actinobacillus pleuropneumoniae, ou Erysipelothrix rhusiopathiae.
Une mortalité massive et collective sur quelques jours peut également être liée à une intoxication ou un empoisonnement.
CRITÈRES DE SUSPICION
Le contexte épidémiologique (absence apparente de facteurs de risque tels qu’introduction d’animaux, contacts avec la faune sauvage, etc.) ne doit pas moduler la déclaration d’une suspicion au risque d’écarter des suspicions par défaut. En effet, par définition, les circonstances d’apparition d’une maladie exotique ne sont pas connues à l’avance.
Les tableaux cliniques et lésionnels de la PPA sont présentés en annexe . Les critères de suspicion clinique de pestes porcines devant faire l’objet d’un signalement immédiat à la direction départementale en charge de la protection des populations (DDecPP) lorsqu’ils sont relevés en élevage sont présentés ci-dessous.
Critères de suspicion clinique en élevage de porcs domestiques
Observation le jour de l’examen ou dans les commémoratifs au cours du mois précédent
de plusieurs animaux dans l’élevage présentant des signes généraux :
- chez les porcs en croissance : appétit diminué, hyperthermie, regroupements des
- animaux, apathie, dyspnée, ataxie, augmentation importante de la consommation d’eau (si mesurable)
- chez les animaux reproducteurs : ces mêmes signes cliniques et/ou des avortements et/ou une forte mortalité sous la mère,
- et/ou lésions hémorragiques externes (rougeurs des extrémités et de la partie déclive de l’abdomen, hémorragies (pétéchies) sur les oreilles et sur le reste du corps),
OU
Enregistrement sur une période de 15 jours d’une mortalité au moins deux fois plus importante que la mortalité moyenne habituellement observée (en excluant les porcelets de moins d’un mois) en prenant en compte la plus petite unité épidémiologique de l’élevage (de la plus petite à la plus grande : salle, bande, atelier).
OU
Observation de lésions internes caractéristiques de PP sur au moins un porc autopsié*.
Les lésions caractéristiques à prendre en compte sont :
- Splénomégalie : rate plus large et/ou de structure modifiée (boueuse, friable), et/ou
- Nœuds lymphatiques hypertrophiés congestionnés, hémorragiques, et/ou
- Rein hypertrophié avec pétéchies, et/ou
- Face interne de la vessie hémorragique.
ET
Absence de diagnostic différentiel (cf. annexe) d’exclusion avéré (identification d’une autre étiologie avec certitude)**.
* Autopsies en élevage est encouragée sans retardent la suspicion de PP basée sur des critères cliniques ou de mortalité, conditions de biosécurité (fiche de bonne pratique d’autopsie SNGTV).
Les autopsies peuvent être réalisées en laboratoire vétérinaire (biosécurité du transport de cadavre
** Attention : concernant le 4ème critère, il conviendra de ne se baser que sur les informations existantes le jour du signalement par le vétérinaire et de ne pas mettre en œuvre d’examens complémentaires qui pourraient retarder l’émission de la suspicion. Pour qu’une suspicion de PP ne soit pas posée suite à l’observation des deux premiers critères, le diagnostic d’exclusion doit être certain. Cela sous-entend que le tableau clinique est caractéristique d’une autre affection, S’il y a le moindre doute, une suspicion de peste porcine doit être posée.
Élevages familiaux :
La présence sur un seul porc ne signes cliniques évocateurs généraux accompagnés de lésions externes voire de lésions internes observés suite à une autopsie doit amener vétérinaire à poser une suspicion de PP et informer la DDCSPP
Critères de suspicion clinique en élevage de sangliers
Mortalités « inhabituelles », non spécifiques d’une tranche d’âge,
OU
Observation le jour de l’examen ou dans les commémoratifs au cours du mois précédent de plusieurs animaux dans l’élevage présentant des signes généraux : comportement lié à l’hyperthermie (ex : recherche de points d’eau), apathie, ataxie.
OU
Observation de lésions internes caractéristiques de PP sur au moins un sanglier autopsié*. Les lésions caractéristiques à prendre en compte sont :
- Splénomégalie : Rate plus large et/ou de structure modifiée (boueuse, friable), et/ou
- Ganglions hypertrophiés congestionnés, hémorragiques, et/ou
- Rein hypertrophié avec pétéchies, et/ou
- Face interne de la vessie hémorragique.
ET
Absence de diagnostic différentiel (cf. annexe 3) d’exclusion avéré (identification d’une autre étiologie avec certitude)**.
PRÉLÈVEMENTS (pour INFO – Soumis à la décision de la DDETSPP)
- toute suspicion entraîne obligatoirement un diagnostic expérimental de certitude.
- en cas de suspicion, prélèvements identiques à ceux de la PPC (reins + rate + ganglions + amygdales + éventuellement sang sur anticoagulant de porcs fébriles pour diagnostic virologique, sang sur tube sec pour diagnostic sérologique).
Le diagnostic expérimental est, selon le cas, virologique et/ou sérologique :





No responses yet